10. Zertan geratzen da egiaztatu
nahi duzun hipotesia V eta N konstante mantentzen badira?
11. Zein esperientzia proposatuko
zenuke hipotesi hori egiaztatzeko?
Irakasleak emango dizu esperientziaren
emaitza, hau da, p/t grafikoa.
12. Zer ondorioztatzen duzu?
Bete al da hipotesia?
Presioa tenperaturarekiko
zuzenki proportzionala ateratzen ez dela ikusita, badirudi
proposatutako hipotesia ez dela zuzena. Proposatu dugun
hipotesia beteko balitz, hau da, p/t grafikoa jatorritik
igaroko balitz, gasaren presioak p = 0 Pa izan beharko
luke bere tenperatura t = 0 °C denean. Eta ez da hala
gertatzen.
Zer egin dezakegu? Hipotesia baztertu? Ala bete dadin
zerbait aldatzen saiatu? Zeren p eta t proportzionalak
izatea guztiz logikoa baitirudi. Goazen, beraz, azken
bide horretan saiatzera.
13. Lehengo p/t grafikoaren
martxa ikusita, zein tenperaturatan izango litzateke zero
gasaren presioa?
Beste
gas-lagin bat hartzen badugu (N eta V desberdinak izango
dira, orokorrean) eta t desberdinentzako p neurtzen badugu,
p/t grafikoa ez da aurrekoa bezalakoa ateratzen, zure
hipotesia betetzen delarik. Izan ere, hipotesiaren arabera
V eta N desberdina duen gasaren p, t jakin batean, desberdina
izango da, eta hala ateratzen da. Baina grafikoa desberdina
izanik ere, aurrekoan bezala gas-lagin berri horren p
zein t-n egingo litzatekeen zero kalkulatuz gero, zuk
lortu duzun balioaren antzekoa ateratzen da, -273 °C
alegia; hala atera zitzaion behintzat Gay-Lussac zientzialari
frantziarrari, gasen presioa eta tenperaturaren arteko
erlazioa ikertzen aritu zenean. Eta gauza bera gertatu
zitzaion edozein gas-laginarekin.
| |
p(atm) |
1. gasa (N1, V2) |
|
|
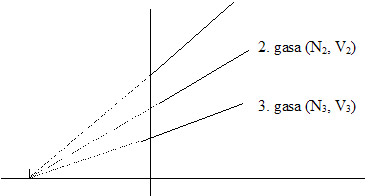
- 273
|
t(°C)
|
Beraz, badirudi t horretan edozein gasaren p zero egingo
litzatekeela, berdin du zein den gasaren N edo V.
14. Posible izango al da
tenperatura hori lortzea? Eta tenperatura horretatik jaistea?
Ez dirudi, ez, -273 °C-eko t lortzea
posible denik. Zeren, nola egon daiteke presiorik egiten
ez duen gasik? Eta are gehiago, tenperatura horren azpitik
presioak negatiboa izan beharko zuen. Ez da posible.
Baina guk zure hipotesiarekin genuen arazoa konpondu
nahian genbiltzan.
15. Zer gertatuko litzateke tenperatura-eskala
aldatu eta eskala berriaren zeroa -273 °C-tan kokatuko
bagenu? Zein tenperaturan egingo litzateke orduan zero
edozein gasaren presioa? Beteko al litzateke orduan gure
hasierako hipotesia?
Gay-Lussacen neurketa eta kalkuluetan oinarrituta,
kimikariek tenperatura-eskalaren jatorria puntu horretara
(-273 °C) eramanez, konturatu egin ziren p zero egiten
dela T zero denean, hau da, p/T grafikoa jatorritik igarotzen
den zuzena dela, p eta T zuzenki proportzionalak direla:
proposatutako hipotesia bete egiten dela, alegia.
Tenperatura-eskala horri, tenperatura absolutua edo tenperatura
termodinamikoa (T, ez t Celsius-eskalan neurtzen denean
bezala) deitzen zaio. Jatorria, esan bezala, -273 °C-tan
dago, eta unitatea Kelvin (K) deitzen da, hau da: 0 K
= -273 °C.
Baieztatu duzun hipotesia Gay-Lussac-en bigarren legea
da:
Gas batek egiten duen presioa tenperatura absolutuarekiko
zuzenki proportzionala da, bolumena eta korpuskulu-kopurua
konstante mantentzen badira:
p = k·T
16. Zein da tenperatura-eskala absolutua
eta Celsius-eskalaren arteko erlazioa?
Eta zein da, bada, Gay-Lussac-en lehen legea?
Ba V eta t-ren arteko erlazioa (p eta N konstanteak izanik)
ezartzen duena. Izan ere, Gay-Lussacek erlazio hau p eta
t-ren artekoa baino lehen ikertu zuen. Goazen gu ere erlazio
hori ikertzera.
17. Nola geratzen da, zure
hipotesiaren arabera, V eta t-ren arteko erlazioa, p eta
N konstante mantenduz gero?
18. Zein muntaketa esperimentala
egin daiteke erlazio hori baieztatzeko?
Egiaztapen esperimentala egiteko dauden
zailtasun teknikoak ez dira samurrak. Gasaren tenperatura
igotzen den heinean presioa konstante mantentzeko, gasari
zabaltzeko aukera utzi behar zaio, baina ihes egin gabe.
Gay-Lussacek 1.802. urtean lortu zuen lehen muntaketa
egokia diseinatzea. Honetan, gasa zeukan ontzia merkurio
tanta batez itxita zegoen hodi graduatuari lotuta zegoen.
Hala, t igo ahala V-ren igoera ikusten zuen, eta p-ren
konstantetasuna igoera minimoarekin desplazatzen zen merkurio
tantak ziurtatzen zuen, hodi graduatua horizontalki kokatzen
baitzen.
Zuk esperientzia bera egingo duzu, baina simulazio baten
bitartez, interneten aurki dezakezun
http://perso.wanadoo.es/cpalacio/LeyCharles2.htm
web orrian.
Bertan "Ley de Charles"
klikatuz gero, U formako hodi graduatua aurkituko duzu.
Hodiaren mutur bat itxita dago, eta bertan airea dago.
Merkurioz mantentzen da itxita gas hori (gasaren N konstante
mantenduko da, beraz), eta beste muturra irekia da. Gero,
termometro batean kurtsorearen bitartez, hodian dagoen
airearen tenperatura igo dezakezu; tenperatura igo ahala,
airea zabaldu egiten da, eta hodian bolumen gehiago hartzen
du.
Orduan arazo txiki bat sortzen da: U formako hodiaren
bi aldeetan merkurioak maila desberdina hartzen du, alde
batean gasak bultzatuta, eta beraz, gasaren p igo egiten
da. Baina Hg- marka duen botoia sakatuz, merkurioa atera
dezakezu hoditik, bi adarretan altuera bera izan arte,
aireak berriro kanpoko eguratsaren p berreskuratu arte.
Horrela ziurta dezakezu p konstante mantentzen dela t
(eta V) igotzen diren bitartean.
Datuak sartuz, grafiko bat lortuko duzu, eta bertan ikusiko
duzu V eta t-ren erlazioa nolakoa den.
19. Zer ondorioztatzen duzu?
Bete al da hipotesia?
Lehengoan gaudela ematen du. V eta t ez
dira zuzenki proportzionalak ateratzen, hau da, V/t grafikoa
zuzena da baina ez da jatorritik igarotzen. Eta lehen
bezala, hori ere ez da hain arraroa. Grafikoa jatorritik
igarota gasaren bolumenak V = 0 ml izan beharko luke bere
tenperatura t = 0 °C denean. Eta zero azpiko tenperaturan
bolumenak negatiboa izan beharko luke. Ez du zentzu handirik.
Hori ikusita, Gay-Lusacek gasaren bolumenak zerorantz
zein tenperaturatan joko zukeen kalkulatu zuen. Horretarako,
grafikoa luzatu egin zuen (benetako neurketarik ez zuen
egin, ezin baitzituen hain tenperatura baxuak lortu )
eta -273 °C-ko tenperaturarentzat bolumena zero egingo
zela ikusi zuen. Gainera, gas kantitate desberdinak erabiltzean
lortutako grafikoak ez ziren berdinak baina antzeko itxura
zeukaten: kasu guztietan, -273 °C-eko tenperaturan
bolumenak zerorantz jotzen zuen.
20. Egiazta ezazu guk lortu
dugun grafikoan ere hori betetzen dela, bolumenak zerorantz
jotzen duela -273 °C-eko tenperaturan.
Beraz, tenperatura-eskalaren jatorria puntu
horretara (-273 °C) eramanez, tenperatura-eskala absolutua
erabiliz, bolumena ere zero egiten da tenperatura zero
denean, V/T grafikoa jatorritik igarotzen den zuzena da,
V eta T zuzenki proportzionalak dira: proposatutako hipotesia
bete egiten da, alegia.
Hau da Gay-Lussac-en lehen legea:
Gas batek betetzen duen bolumena tenperatura absolutuarekiko
zuzenki proportzionala da, presioa eta korpuskulu-kopurua
konstante mantentzen badira:
V = k·T